|
Graves疾病管理新工具---TSI检测Graves病与TSI 甲状腺功能亢进,简称甲亢,是因甲状腺腺体本身产生甲状腺激素过多而引起的甲状腺毒症。在一项我国十个城市甲状腺疾病流行率的调查研究中显示,甲亢(包括亚临床甲亢)的患病率为1.6%。引起甲亢的病因很多,包括Graves病、多结节性甲状腺肿伴甲亢、甲状腺自主性高功能腺瘤等。其中以Graves病最为常见,占所有甲亢的85%左右。 Graves病临床表现及体征主要有:易激动、烦躁、心悸、怕热多汗等,大多数患者有程度不等的甲状腺肿大。心血管系统表现有心率增快、心脏扩大、心率失常。一部分患者眼部表现为浸润性突眼,也称为Graves眼病或Graves眶病。 Graves病普遍认可的发病机制包括外界感染、遗传、精神创伤诱发免疫功能紊乱,促甲状腺激素受体刺激性抗体(TSI)是Graves病的致病性抗体。TSI与促甲状腺激素受体(TSHR)结合,模拟促甲状腺激素(TSH)对甲状腺的刺激作用,诱导甲状腺激素T3,T4合成分泌增加,同时TSI与促甲状腺激素受体(TSHR)的结合不受负反馈调控,最终导致Graves病。
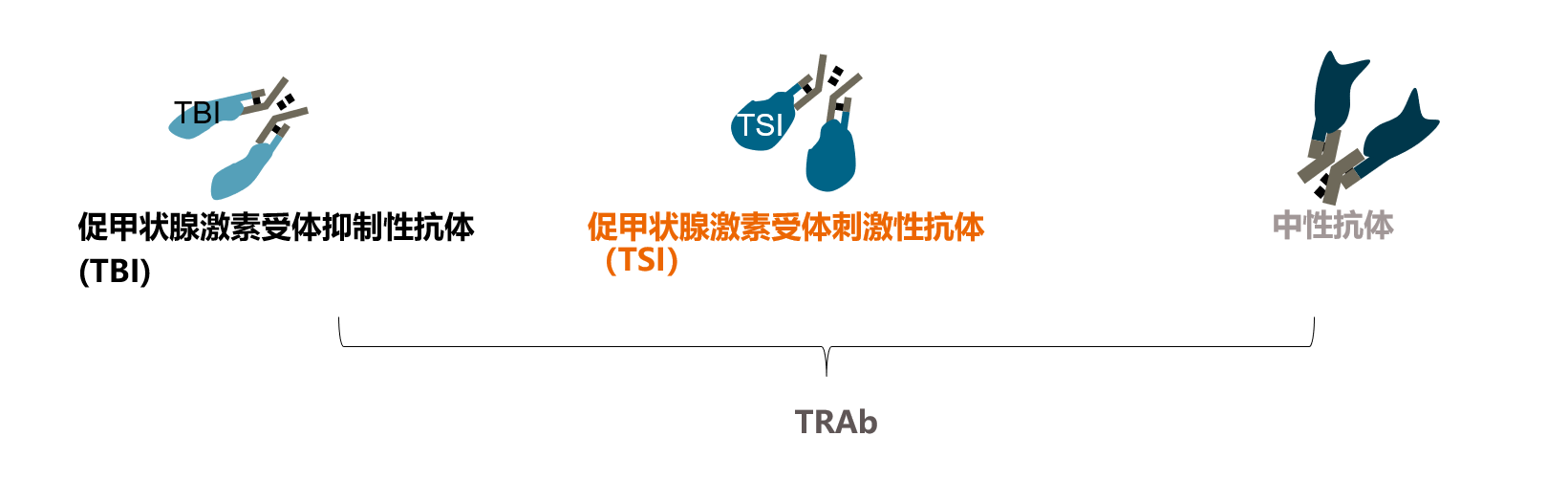
TSI检测技术的发展 生理情况下,TSH通过与甲状腺滤泡细胞膜表面的TSHR结合,调节甲状腺激素的合成和分泌。当在遗传、环境及其他自身免疫性疾病发生时,由B淋巴细胞产生特异的免疫球蛋白TSH受体抗体,即促甲状腺激素受体抗体(TRAb)。TRAb是一种多克隆抗体,根据功能分为包括:促甲状腺激素受体刺激性抗体(TSI)、促甲状腺激素受体抑制性抗体(TBI)以及中性抗体。 TSI、TBI都可以与TSH受体结合,但是对于甲状腺功能产生的影响却是完全不同的。TSI与TSH受体结合, 模拟促甲状腺激素TSH对甲状腺的刺激作用,导致Graves甲亢。与TSI 相反, TBI 与TSH受体结合,抑制促甲状腺激素TSH对甲状腺的刺激作用,导致甲状腺功能减退。既往没有TSI检测商品化的试剂盒,临床应用较多的是TRAb检测试剂盒,但是TRAb检测不能区分抗体类型。如果可以将不同的抗体进行分开检测,那么就可以帮助临床对甲状腺疾病进行更加精准的评估。 有研究认为TSI 主要识别 TSH受体胞外域 N 端的构象性表位,TBI 主要识别 TSH受体胞外域 C 端的线性表位。Mc4 是近些年广泛应用的重组人 TSH受体嵌合体,它保留了 TSI位点的激动刺激活性,并以大鼠黄体生成素-绒毛膜促性腺激素(LH-CG)受体代替 TBI主要的结合位点。
TSI、TBI都可以与TSH受体结合,但是对于甲状腺功能产生的影响却是完全不同的。TSI与TSH受体结合, 模拟促甲状腺激素TSH对甲状腺的刺激作用,导致Graves甲亢。与TSI 相反, TBI 与TSH受体结合,抑制促甲状腺激素TSH对甲状腺的刺激作用,导致甲状腺功能减退。既往没有TSI检测商品化的试剂盒,临床应用较多的是TRAb检测试剂盒,但是TRAb检测不能区分抗体类型。如果可以将不同的抗体进行分开检测,那么就可以帮助临床对甲状腺疾病进行更加精准的评估。 有研究认为TSI 主要识别 TSH受体胞外域 N 端的构象性表位,TBI 主要识别 TSH受体胞外域 C 端的线性表位。Mc4 是近些年广泛应用的重组人 TSH受体嵌合体,它保留了 TSI位点的激动刺激活性,并以大鼠黄体生成素-绒毛膜促性腺激素(LH-CG)受体代替 TBI主要的结合位点。
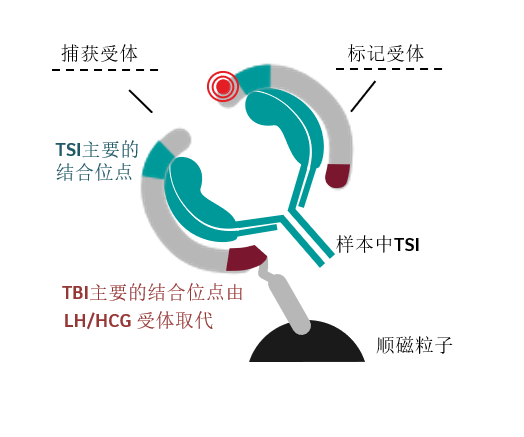
图1.野生型TSH受体与Mc4嵌合受体示意图 TSI检测建立了一种生物分析法,样本中TSI与TSH受体嵌合体结合,模拟TSH的作用,引起细胞内腺苷酸环化酶活化,使得环磷酸腺苷(cAMP)浓度增高,通过检测cAMP 的水平来检测TSI。此方法操作繁琐,费用高,主要用于科研。 近年来,西门子医疗推出了首个使用化学方法检测TSI的试剂盒,这一创新的检测技术,使得TSI检测的应用从科研走向了临床。试剂盒采用一对TSH受体嵌合体(捕获受体与标记受体),捕获受体固定于固相,样本中的TSI通过一个臂与捕获受体结合,通过二臂与标记受体结合,然后进行化学发光反应,从而对TSI进行定量检测。
图2.TSI检测原理示意图 ·试剂盒中重组的人TSH受体嵌合体对TSI进行特异性捕获和检测。 ·由于去除了TBI主要的结合位点,使得TBI对于检测的影响最小化。 TSI检测试剂盒的基本信息
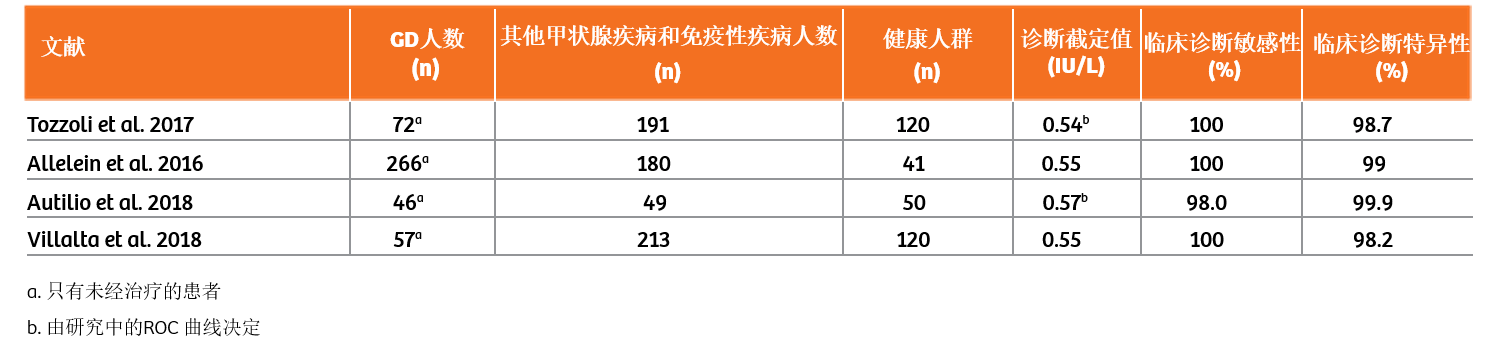
TSI检测的临床应用 1.Graves病的诊断、治疗后停药及复发预测 目前已经有多篇文献对西门子医疗IMMULITE2000 TSI的试剂盒进行了评估,TSI检测在Graves病中诊断的敏感性和特异性都在98%以上[1,2,3,4]。文献中纳入的评估人群包括Graves病、干扰疾病(其他甲状腺疾病和免疫性疾病人群)以及健康人群。
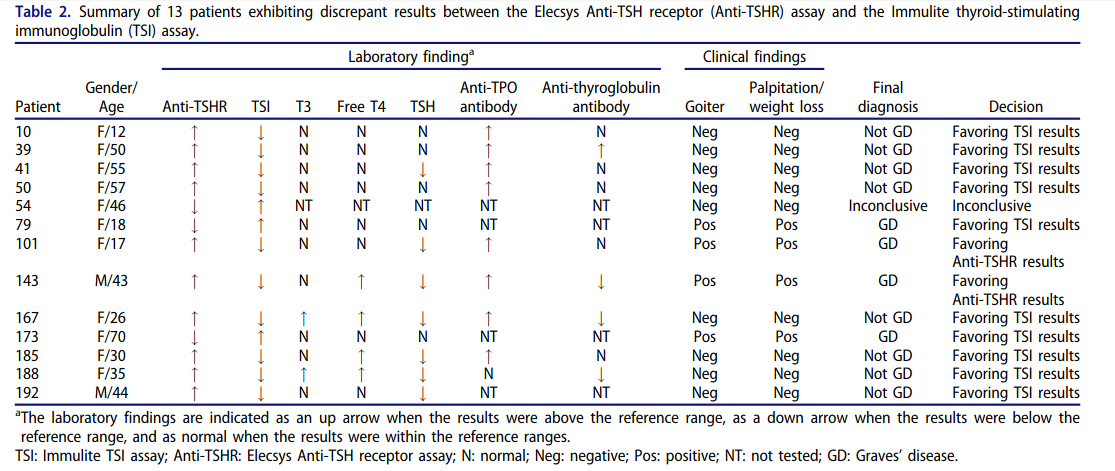
表1.TSI检测相关文献汇总 一篇已发表文献收集了187例甲状腺疾病患者血清样本,同时进行TSI与TRAb检测,根据检测结果计算两者的一致性。同时对于不一致样本,进行回顾性分析,收集患者的临床信息,依据指南诊断标准,进行临床判断,评估哪一种检测结果与临床诊断更加一致。结果显示,两种检测方法一致率为93%。对于其中13例不一致样本进行临床评估,其中10例样本临床诊断与TSI结果一致:8例是TSI检测结果阴性而TRAb结果阳性,患者的临床诊断结果显示不是Graves病,主要是桥本甲状腺炎、甲状腺结节和妊娠期甲状腺毒症等,另外2例是TSI检测结果阳性而TRAb结果阴性,患者的临床诊断为Graves病。[5]
图3. 13例检测结果不一致样本的信息汇总 2.Graves眼病 Graves 眼病是Graves病最常见的一种甲状腺腺外表现,其早期组织学变化为大量淋巴细胞浸润、氨基葡聚糖沉积和水肿。晚期则表现为眼球后组织纤维化。25%~50%的Graves病患者伴有不同程度的眼病,而5%仅有明显突眼而无甲亢症状,称为甲状腺功能正常的Graves眼病。有学者把TSI称为“Graves眼病的功能性标志物”,发现TSI和Graves眼病的活动性(r=0.83, P<0.001)和严重度(r=0.81, P<0.001)密切相关。而TRAb与眼病活动性(r=0.23, P=0.016) 和 严重性 (r=0.21, P=0.029)弱相关[6]。
3.妊娠期女性及新生儿甲亢 妊娠一过性甲状腺毒症在妊娠妇女中的发生率越约2%-3%,临床表现为甲亢症状,病情的程度与血清hcG水平增高程度相关,但是无突眼,TSI阴性。TSI的检测是鉴别妊娠一过性甲状腺毒症和妊娠Graves病的重要手段。 既往有甲亢史的孕妇所生的新生儿约有1%-5%会发生新生儿甲亢,TSI可以通过胎盘屏障影响新生儿的甲状腺功能。在妊娠期进行TSI检测,是新生儿甲亢的的预测指标。有研究表明,在妊娠晚期基于生物检测法的TSI结果>5IU/L 时,对于新生儿甲亢的预测敏感性和特异型分别为100%和76%[7]。 西门子医疗IMMULITE 2000 TSI检测试剂盒,以其特色的检测技术、优异的试剂性能,使得TSI检测从幕后走到台前,为Graves病患者疾病管理开启了新的篇章。
参考文献: [1] Renato Tozzoli et al. Evaluation of the first fully automated immunoassay method for the measurement of stimulating TSH receptor autoantibodies in Graves’ disease. Clinical Chemistry & Laboratory Medicine, 2016. 55(1). [2]..Allelein et al., Clinical Evaluation of the First Automated Assay for the Detection of Stimulating TSH Receptor Autoantibodies.Horm Metab Res 2016;48:795–801 [3].Autilio et al., Stimulating TSH receptor autoantibodiesimmunoassay: analytical evaluation and clinical performance in Graves’ disease Ann Clin Biochem 2018, Vol. 55(1) 172–177 [4].Villalta et al., Diagnostic accuracy of a new fluoroenzyme immunoassay for the detection of TSH receptor autoantibodies in Graves’ disease .Auto Immun Highlights 2018;9. [5]. Kim J J , Jeong S H , Kim B , et al. Analytical and clinical performance of newly developed immunoassay for detecting thyroid-stimulating immunoglobulin, the IMMULITE TSI assay[J]. Scandinavian Journal of Clinical and Laboratory Investigation. 2019,79:6, 443-448, [6]. Katharina A. Ponto, MD, et al. Clinical Relevance of Thyroid-Stimulating Immunoglobulins in Graves’ Ophthalmopathy [J]. American Academy of Ophthalmology. 2011, Vol. 18(11) 2279–2285 [7]. Peleg D , Cada S , Peleg A , et al. The relationship between maternal serum thyroid-stimulating immunoglobulin and fetal and neonatal thyrotoxicosis[J]. Obstetrics & Gynecology, 2002, 99(6):0-1043. 本文转载自医学仪器与试剂网 |